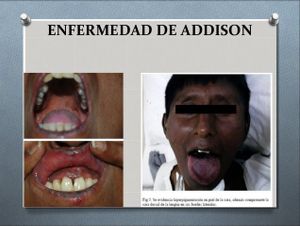
La enfermedad de Addison es un trastorno hipofuncionante insidioso y en general progresivo de la corteza suprarrenal que provoca diversos síntomas, como hipotensión arterial e hiperpigmentación.
Puede desencadenar una crisis suprarrenal con colapso cardiovascular.
El diagnóstico es clínico y se basa en el hallazgo de concentraciones plasmáticas elevadas de ACTH con concentraciones plasmáticas bajas de cortisol.
El tratamiento depende de la causa, pero suele realizarse con hidrocortisona y, en ocasiones, otras hormonas.
La enfermedad de Addison se desarrolla en alrededor de 4/100.000 individuos por año.
Se identifica en personas de todas las edades, con una incidencia equivalente en ambos sexos y una tendencia a manifestarse clínicamente durante situaciones de tensión metabólica o traumatismos.
El establecimiento de síntomas graves (crisis suprarrenal) puede precipitarse ante una infección aguda (causa frecuente, en especial con septicemia).
Otras causas incluyen traumatismos, cirugía y pérdida de sodio debido a sudoración excesiva. Con el tratamiento, la enfermedad de Addison no debe reducir la expectativa de vida.
Etiología
En los Estados Unidos, alrededor del 70% de los pacientes con enfermedad de Addison presenta atrofia idiopática de la corteza suprarrenal, que puede ser secundaria a procesos autoinmunitarios.
El resto se debe a la destrucción de la corteza suprarrenal por un granuloma (p. ej., tuberculosis), un tumor, amiloidosis, una hemorragia o necrosis inflamatoria.
El hipofuncionamiento de la corteza suprarrenal también puede deberse a la administración de fármacos que bloquean la síntesis de corticoides (p. ej., ketoconazol, el anestésico etomidato).
La enfermedad de Addison puede coexistir con diabetes melitus o hipotiroidismo en pacientes con síndrome de deficiencia poliglandular (ver Síndromes de deficiencias poliglandulares). En los niños, la causa más frecuente de insuficiencia suprarrenal primaria es la hiperplasia suprarrenal congénita (ver Hiperplasia suprarrenal congénita).
Fisiopatología
Se identifican deficiencias tanto de mineralocorticoides como de glucocorticoides.
Deficiencia de mineralocorticoides
Dado que los mineralocorticoides estimulan la reabsorción de sodio y la excreción de potasio, su deficiencia aumenta la excreción de sodio y disminuye la de potasio, principalmente en la orina, aunque también en el sudor, la saliva y el tubo digestivo.
En consecuencia, el paciente presenta hiponatremia e hiperpotasemia.
La incapacidad de concentrar la orina, combinada con los desequilibrios electrolíticos, causa deshidratación grave, hipertonicidad del plasma, acidosis, hipovolemia, hipotensión arterial y, por último, colapso circulatorio. No obstante, cuando la insuficiencia suprarrenal es secundaria a una producción inadecuada de ACTH (insuficiencia suprarrenal secundaria, ver Insuficiencia suprarrenal secundaria), las concentraciones de electrolitos suelen ser normales o sólo están levemente alteradas.
Deficiencia de glucocorticoides
La deficiencia de glucocorticoides contribuye al desarrollo de hipotensión arterial y aumenta en forma significativa la sensibilidad a la insulina , además de generar trastornos en el metabolismo de los hidratos de carbono, los lípidos y las proteínas.
En ausencia de cortisol, se sintetiza una cantidad insuficiente de hidratos de carbono a partir de las proteínas, con generación de hipoglucemia y disminución de las reservas hepáticas de glucógeno.
A continuación se desarrolla debilidad, en parte debido a la función neuromuscular deficiente. La resistencia a las infecciones, los traumatismos y otras tensiones está disminuida. La debilidad miocárdica y la deshidratación reducen el gasto cardíaco y el paciente puede presentar una insuficiencia circulatoria.
La reducción de la cortisolemia estimula la producción hipofisaria de ACTH y aumenta la concentración sanguínea de β-lipotropina, que tiene actividad estimulante de los melanocitos y, junto con la ACTH, causa la hiperpigmentación de la piel y de las mucosas característica de la enfermedad de Addison. Por lo tanto, la insuficiencia suprarrenal secundaria a una insuficiencia hipofisaria (ver Insuficiencia suprarrenal secundaria) no causa hiperpigmentación.
Signos y síntomas
La debilidad, el cansancio y la hipotensión ortostática son signos y síntomas tempranos. La hiperpigmentación se caracteriza por bronceado extenso de las porciones expuestas del cuerpo y en menor medida de las no expuestas, en especial las áreas que soportan presión (prominencias óseas), la piel, las cicatrices y las superficies extensoras.
Con frecuencia se identifican efélides o pecas de color oscuro en la frente, la cara, el cuello y los hombros. También aparecen áreas de vitiligo, además de cambios de coloración negro-azuladas en las aréolas y las mucosas de los labios, la boca, el recto y la vagina.
Los pacientes suelen presentar anorexia, náuseas, vómitos y diarrea. También puede informarse una disminución de la tolerancia al frío, con hipometabolismo. El paciente puede presentar vértigo y síncope.
El establecimiento gradual y la naturaleza inespecífica de los síntomas tempranos suelen confundir el diagnóstico inicial con la neurosis. La pérdida de peso, la deshidratación y la hipotensión arterial son características de los estadios más avanzados de la enfermedad de Addison.
Crisis suprarrenal
La crisis suprarrenal se caracteriza por astenia profunda, dolor intenso en el abdomen, la región lumbar o las piernas, colapso vascular periférico y, por último, disfunción renal con uremia. La temperatura corporal puede ser baja, aunque en ocasiones los pacientes desarrollan fiebre elevada, en particular cuando la crisis es desencadenada por una infección aguda. Un número significativo de pacientes con pérdida parcial de la función suprarrenal (reserva adrenocortical limitada) se encuentra bien, pero cuando se expone a un estrés fisiológico (p. ej., cirugía, infección, quemaduras, enfermedades críticas) experimenta una crisis suprarrenal. El shock y la fiebre pueden ser los únicos signos.
Diagnóstico
Electrolitos
Concentración sérica de ACTH
En ocasiones, prueba de estimulación con ACTH
Los signos y los síntomas clínicos sugieren una insuficiencia suprarrenal. En ocasiones, el diagnóstico sólo se considera al observar las alteraciones características en las concentraciones séricas de electrolitos, por ejemplo hiponatremia (< 135 mEq/L), hiperpotasemia (> 5 mEq/L), concentración de bicarbonato disminuida (HCO3) (15 a 20 mEq/L) y aumento de la concentración de nitrógeno ureico en sangre (véase Resultados de las pruebas que sugieren una enfermedad de Addison).
Resultados de las pruebas que sugieren una enfermedad de Addison
Prueba
Panel químico en sangre
Índice Na:K sérico
Glucemia, en ayunas
< 50 mg/dL (< 2,78 mmol/L)
HCO3 plasmático
< 15–20 mEq/L
Nitrógeno ureico en sangre
> 20 mg/dL (> 7,1 mmol/L)
Hematología
Recuento de leucocitos
Linfocitosis relativa
Eosinófilos
Estudios de diagnóstico por la imagen
Calcificaciones en el área suprarrenal
Tuberculosis renal
Tuberculosis pulmonar
Diagnósticos diferenciales
El carcinoma broncogénico, la ingestión de metales pesados (p. ej., hierro, plata), las dermopatías crónicas o la hemocromatosis producen hiperpigmentación.
El síndrome de Peutz-Jeghers se caracteriza por pigmentación de las mucosas yugal y rectal. Los pacientes con vitiligo muchas veces desarrollan hiperpigmentación, en cuyo caso puede sospecharse una enfermedad de Addison, aunque otras enfermedades también pueden presentar esta asociación.
La debilidad generada por la enfermedad de Addison disminuye con el reposo, a diferencia de la asociada con trastornos neuropsiquiátricos, que con frecuencia es peor durante la mañana que después de la actividad. La mayoría de las miopatías que causan debilidad pueden distinguirse por su distribución, la ausencia de pigmentación anormal y el hallazgo de pruebas de laboratorio características.
Los pacientes con insuficiencia suprarrenal desarrollan hipoglucemia después del ayuno debido a la reducción de la gluconeogénesis. En cambio, los pacientes con hipoglucemia secundaria a la secreción excesiva de insulina pueden presentar una crisis en cualquier momento, en general tienen mayor apetito y ganan peso y pueden presentar una función suprarrenal normal.
La hiponatremia causada por la enfermedad de Addison debe distinguirse de la identificada en pacientes edematizados con cardiopatía o hepatopatía (en particular en los que reciben diuréticos), de la hiponatremia dilucional del síndrome de secreción inapropiada de ADH y de la nefritis perdedora de sal. Estos pacientes no suelen presentar hiperpigmentación, hiperpotasemia ni aumento de la concentración de nitrógeno ureico en sangre.
Evaluación
Las pruebas de laboratorio, que deben comenzar con concentraciones sanguíneas de cortisol y ACTH, confirman la insuficiencia suprarrenal. El aumento de la concentración de ACTH (≥ 50 pg/mL) con hipocortisolemia (< 5 μg/dL [< 138 nmol/L]) permite confirmar el diagnóstico, sobre todo en pacientes sometidos a tensiones intensas o en estado de shock. Las concentraciones bajas de ACTH (< 5 pg/mL) y cortisol sugieren una insuficiencia suprarrenal secundaria (ver Insuficiencia suprarrenal secundaria). Debe destacarse que es imposible hallar concentraciones normales de ACTH cuando la cortisolemia es muy baja.
Si las concentraciones de ACTH y cortisol son limítrofes y se sospecha una insuficiencia suprarrenal de acuerdo con la evaluación clínica, en particular en un paciente que va a ser sometido a una cirugía mayor, hay que pedir una prueba de provocación. Si se cuenta con muy poco tiempo (p. ej., cirugía de urgencia), el paciente debe recibir hidrocortisona empírica (p. ej., 100 mg por vía intravenosa o intramuscular).
La enfermedad de Addison se diagnostica cuando se observa que la administración de ACTH exógena no es capaz de aumentar la cortisolemia.
La insuficiencia suprarrenal secundaria se diagnostica cuando se detecta una prolongación en la prueba de estimulación con ACTH, la prueba de tolerancia a la insulina o la prueba de glucagón.
La prueba de estimulación con ACTH consiste en la inyección de 250 μg de cosintropina (ACTH sintética) por vía intravenosa o intramuscular. Algunos expertos creen que en los pacientes en los que se sospecha insuficiencia suprarrenal secundaria debe indicarse una prueba de estimulación con una dosis baja de ACTH (1 μg por vía intravenosa en lugar de la dosis estándar de 250 μg), porque estos pacientes pueden reaccionar con resultados normales al administrar dosis más altas.
Los pacientes tratados con suplementos de glucocorticoides o espironolactona no deben recibirlos el día de la prueba. El rango normal de cortisolemia previa a la inyección oscila entre 5 y 25 μg/dL (entre 138 y 690 nmol/L) y se duplica en 30 a 90 minutos, para alcanzar al menos 20 μg/dL (552 nmol/L).
Los pacientes con enfermedad de Addison presentan concentraciones bajas o normales-bajas que no aumentan por encima de 20 μg/dL a los 30 minutos. Puede observarse una respuesta normal al cosintropina en pacientes con insuficiencia suprarrenal secundaria.
No obstante, como la insuficiencia hipofisaria puede producir una atrofia suprarrenal (y por ende, una incapacidad para responder a la ACTH), el paciente puede requerir cebado suprarrenal, con 1 mg de ACTH de acción prolongada una vez al día 3 días antes de la prueba si se sospecha una enfermedad hipofisaria.
Una prueba de estimulación con ACTH prolongada (muestra de 24 horas) puede servir para diagnosticar una insuficiencia suprarrenal secundaria (o terciaria, es decir, de origen hipotalámico).
En ese caso, debe administrarse 1 mg de cosintropina por vía intramuscular para medir la cortisolemia cada 24 horas.
Los resultados de la primera hora son similares en la prueba corta (se suspende la recolección de la muestra después de 1 hora) y en las pruebas prolongadas, pero en la enfermedad de Addison no se observa un aumento adicional después de los primeros 60 minutos. En la insuficiencia suprarrenal secundaria y terciaria, la cortisolemia continúa en aumento durante ≥ 24 horas. Sólo cuando existe atrofia suprarrenal de larga data debe administrarse cebado suprarrenal (con ACTH de larga duración). La prueba corta simple suele indicarse en primer lugar, porque una respuesta normal evita la necesidad de otras evaluaciones.
Si se sospecha una crisis suprarrenal, la confirmación de la enfermedad de Addison con estimulación con ACTH se retrasa hasta la recuperación del paciente.
Si se evalúa la estimulación con ACTH, el aumento de la concentración de ACTH junto con la disminución de la cortisolemia confirman el diagnóstico.
En las sociedades occidentales, la causa suele asumirse como autoinmunitaria, salvo que se evidencie lo contrario. Pueden buscarse autoanticuerpos suprarrenales y debe solicitarse una radiografía de tórax para detectar tuberculosis.
En caso de duda, la tomografía computarizada (TC) de las glándulas suprarrenales puede ser útil. En los pacientes con enfermedad autoinmunitaria, las glándulas suprarrenales están atrofiadas, mientras que en aquellos con tuberculosis u otros granulomas, las glándulas suprarrenales están aumentadas de tamaño (en el período inicial) con calcificaciones frecuentes. La hiperplasia suprarrenal bilateral sugiere un defecto enzimático.
Tratamiento
Hidrocortisona o prednisona
Aumento de la dosis durante enfermedades intercurrentes
En condiciones normales, la concentración máxima de cortisol se secreta durante la mañana y la concentración mínima, durante la noche. En consecuencia, la hidrocortisona (idéntica al cortisol) debe administrarse en 2 o 3 dosis divididas, con dosis diarias totales de entre 15 y 30 mg.
Un régimen consiste en la administración de la mitad de la dosis durante la mañana y la otra mitad dividida entre la hora del almuerzo y la tarde (p. ej., 10, 5 y 5 mg). Otros profesionales administran dos terceras partes de la dosis por la mañana y una tercera parte por la tarde. Deben evitarse las dosis justo antes de acostarse porque pueden causar insomnio.
En forma alternativa, puede indicarse la administración de 5 mg de prednisona por vía oral durante la mañana y 2,5 mg por vía oral por la tarde. Asimismo, se recomienda el aporte de 0,1 a 0,2 mg de fludrocortisona por vía oral para reponer la aldosterona. La forma más sencilla de ajustar la dosis consiste en confirmar que la concentración de renina se encuentre dentro del rango normal. La hidratación normal y la ausencia de hipotensión ortostática indican que la terapia de reposición es adecuada. En algunos pacientes, la fludrocortisona causa hipertensión arterial, que se trata con reducción de la dosis o mediante la administración de un antihipertensivo no diurético. Algunos médicos tienden a usar una dosis demasiado baja de fludrocortisona en un esfuerzo por evitar el uso de antihipertensivos.
Las enfermedades intercurrentes (p. ej., infecciones) pueden ser graves y deben tratarse de manera exhaustiva. La dosis de hidrocortisona que recibía el paciente debe duplicarse durante esta enfermedad. Si las náuseas y los vómitos contraindican la administración por vía oral, debe implementarse terapia parenteral. Es necesario indicar suplementos de prednisona, y los pacientes deben aprender a autoadministrarse la hidrocortisona por vía parenteral en situaciones urgentes.
El paciente debe tener acceso inmediato a una jeringa precargada con 100 mg de hidrocortisona. Un brazalete o una tarjera en la billetera donde se informe el diagnóstico y la dosis de corticoides puede ser útil frente a una crisis suprarrenal que le impida al paciente comunicarse. Cuando la pérdida de sal es significativa, como en los climas muy cálidos, la dosis de fludrocortisona puede tener que aumentarse.
Cuando la enfermedad de Addison coexiste con diabetes mellitus, la dosis de hidrocortisona no debe ser > 30 mg/día, porque pueden aumentar los requerimientos de insulina .
Tratamiento de las complicaciones
En ocasiones, se desarrolla fiebre > 40,6° C durante el proceso de rehidratación. Salvo en presencia de hipotensión arterial, pueden administrarse con precaución antipiréticos (p. ej., 650 mg de aspirina) por vía oral.
Las complicaciones de la terapia con corticoides pueden incluir reacciones psicóticas, que si se desarrollan después de las primeras 12 horas de iniciado el tratamiento, requieren una reducción de la dosis de hidrocortisona hasta el nivel más bajo que permita mantener la tensión arterial y un funcionamiento cardiovascular adecuado. Pueden requerirse antipsicóticos en forma temporaria, pero su empleo no debe prolongarse.